Volumen 35, Nº 1 | 2017
Paciente de 40 años con insuficiencia cardíaca aguda - 40-year-old patient with acute heart failure Discussion
Carlos Estrada Moderator: Modera: Pablo Lemos Pathology: Candelaria Mendoza Molecular biology: Ariel Sánchez
Palabras clave:
Keywords:
DISCUSIÓN CLÍNICA
Se trata de una paciente de 49 años de edad, que como antecedentes personales sólo recabamos que el padre tenía enfermedad coronaria y su madre era hipertensa. No tenía otros factores de riesgo cardiovascular. En general es una paciente sana, hasta 8 días antes del ingreso tenía actividad física regular.
Ocho días antes de su ingreso comienza con tos seca, fiebre y disnea clase funcional I. A los 5 o 6 días progresa a clase funcional II y IV y es internada en una terapia intensiva de la ciudad de Morteros. Inicialmente con tratamiento con vasodilatadores y diuréticos, relativamente estable. Mientras estaba almorzando, sufre una fibrilación ventricular, según nos cuentan presenciada pero tiene una reanimación de al menos 30 minutos. Sale del evento con ritmo sinusal pero ya en shock cardiogénico con necesidad de drogas vasopresoras.
En esa instancia comienza a gestionarse el traslado a nuestra institución. En el transcurso de su traslado desde Morteros a Córdoba sufre otro episodio de paro cardíaco. También nos informan que presentaba problemas con la ventilación y oxigenación. Quizá ahí, más que en el primer episodio, es cuando sufre los daños cerebrales hipóxicos severos. Llega a nuestro Hospital, es internada rápidamente en la Unidad Coronaria y al poco tiempo de estar en la Unidad Coronaria vuelve a presentar otro episodio de fibrilación ventricular, es reanimada, y sale con taquicardia sinusal pero con shock cardiogénico bien instalado con alta necesidad de drogas vasopresoras.
Se le colocó un catéter de Swan-Ganz que tenía un patrón cardiogénico inicial, y posteriormente como no respondía a las drogas vasopresoras y mínimas dosis de inotrópicos que le permitían, se instaló un balón de contrapulsación aórtica. Dada la gravedad de sus lesiones neurológicas valoradas inicialmente, no la incluimos en una lista de urgencia de trasplante cardíaco. La paciente progresa rápidamente a falla multiorgánica y fallece.
Vamos a analizar a esta paciente con un diagnóstico sindrómico enfocándola en lo que se refiere a insuficiencia cardíaca aguda (ICA). Para ello tenemos que descartar varias causas y después concentrarnos en lo que probablemente haya ocurrido con la paciente.
Primero, cuáles son las causas probables de ICA: la hipertensión arterial en su forma de presentación de crisis hipertensiva o emergencia hipertensiva, con claudicación aguda del ventrículo izquierdo de desarrollo de edema agudo de pulmón. Las valvulopatías, sobre todo las valvulopatías mitrales o la disfunción valvular, ya sea por endocarditis o lo que sea de instalación aguda, cosa que para esto teníamos que valorar el ecocardiograma que se realizó. En los contextos mencionados, la paciente no tenía antecedentes de hipertensión, era una mujer sana, no se le conocía consultas médicas previas, no tenía historia de valvulopatía ni de enfermedad reumática conocida.
La otra causa de ICA es la reagudización de una insuficiencia cardíaca crónica (ICC), producida por poca adherencia a veces al tratamiento, transgresiones dietéticas, y puede ocurrir también un síndrome coronario agudo (SCA), insertado en el contexto de ICC que puede reagudizar la insuficiencia cardíaca. Lo más importante a descartar en estos casos es el SCA. Esta paciente no tenía factores de riesgo para enfermedad coronaria. De todas formas no tenía el electro las características típicas de un infarto, con supra ST o infra ST. La curva de enzimas y la troponina T no había una curva evolutiva compatible, y como dije no tenía factores de riesgo y no había tenido clínica de presentación como un infarto agudo.
Las otras causas que no sean por enfermedad coronaria, como por ejemplo el síndrome de Takotsubo que puede presentarse también como un infarto y puede evolucionar rápidamente al shock cardiogénico, pero tampoco tenía las características ecocardiográficas de lo que se ve en un síndrome de Takotsubo que es la disquinesia apical.
Nos queda finalmente el capítulo de las afecciones propias del músculo cardíaco, entre ellas las miocarditis. Siempre la miocarditis es un desafío diagnóstico por la heterogeneidad de las presentaciones clínicas que tienen. Algunos datos son importantes: en los pacientes jóvenes con muerte súbita la prevalencia está entre el 2 y el 42%, hay pacientes adultos que tienen miocardiopatía dilatada, inexplicable e idiopática, y en la biopsia endomiocárdica el 9 al 16% tienen miocarditis. Es más común en los niños, que tienen miocardiopatía dilatada, más o menos el 46% son post-miocarditis. Hay un 30% de los pacientes que tienen miocarditis que desarrollan posteriormente miocardiopatía dilatada.
Desde 1990 hasta 2015, el número de muertes por miocarditis y cardiomiopatías es de alrededor 180.000 mil en los hombres y en las mujeres alrededor de 140.000. Si esto lo tomamos en índices de muertos por cada 100.000 habitantes, en los hombres es 5.5 por cada 100.000 y las mujeres alrededor 4.2 por cada 100.000 habitantes.
Es a veces difícil definir el diagnóstico de miocarditis. En realidad es una definición histológica y se trata como dijimos de una inflamación del miocardio y que está establecido por criterios histológicos, algunos inmunológicos e inmunohistoquímicos. Los histológicos están dados por los criterios de Dallas que considera una infiltración linfocitaria y además de eso hay degeneración y necrosis de los miocitos y también se describe la miocarditis border line que es sólo la infiltración linfocitaria del miocardio, sin necrosis de los miocitos. Hay también criterios inmunohistoquímicos no específicos que se caracteriza por lo siguiente, por ejemplo la presencia de más de 14 leucocitos mm2, incluyendo hasta 4 monocitos por mm2 con el uso o presencia de marcadores como CD3 linfocitos T.
¿Cómo es la presentación de la miocarditis? Existe lo que se llama, como dijimos, la heterogeneidad de la presentación clínica que es muy importante. Tenemos desde síntomas muy leves que son dolor de pecho, leve disnea y deterioro leve de la función sistólica hasta el otro extremo, que son pacientes que en poco tiempo, como ocurrió con esta paciente, desarrollan ICA, deterioro severo del estatus hemodinámico y shock cardiogénico. En este contexto se inscribe lo que se denomina miocarditis fulminante y se caracteriza porque tiene un rápido comienzo, suelen tener fiebre o severo compromiso hemodinámico, ICA y shock cardiogénico. Después están los cuadros subagudos, las miocarditis subagudas, donde los síntomas como dijimos son del otro extremo. Son síntomas mucho más leves y tienen deterioro leve a moderado de la función sistólica.
En relación a la miocarditis crónica, si progresan los fenómenos inflamatorios o autoinmunes, o sigue la persistencia de las replicaciones virales, se desarrolla lo que es la miocarditis crónica con disfunción sistólica, remodelado del ventrículo izquierdo y progresa a la miocardiopatía dilatada.
Cuáles son los criterios diagnósticos para sospechar una miocarditis. La clínica más o menos lo dijimos, son los dolores precordiales, a veces están incluidos los dolores pericárdicos que son pseudoisquémicos, pueden ser de reciente inicio, que se toman entre pocos días hasta 3 meses o síntomas más subagudos o crónicos cuando es mayor de tres meses y se refiere a los grados de disfunción sistólica con disnea progresiva. También refieren palpitaciones, arritmias ventriculares y se pueden presentar también como un shock cardiogénico de origen no explicado. Los criterios diagnósticos por ejemplo para el electrocardiograma son variados. Puede haber trastornos de conducción con bloqueos de primero hasta tercer grado, puede haber alteraciones del ST que pueden ser infradesnivel o supradesnivel, que habitualmente cuando hay compromiso difuso en el ecocardiograma y compromiso del pericardio puede haber supradesnivel del ST y en este caso hay que descartar firmemente la presencia de los SCA y las arritmias ventriculares, que pueden ser de distinta gravedad. Pueden ser taquicardias ventriculares, también puede tener taquicardias supraventriculares o debutar con fibrilación ventricular.
Los marcadores de necrosis muscular como siempre son la troponina T y la troponina I que tienen valores elevados y valoramos las imágenes que es la que nos sirve para descartar otras causas de ICA como puede ser el ecocardiograma, la angiografía o la resonancia nuclear magnética (RNM). Con respecto al ecocardiograma nos sirve para descartar valvulopatías, anormalidades de la contracción regional si hay sospecha de la presencia de un SCA, descartar miocardiopatías sobre todo del tipo hipertróficas. De forma importante lo que se ve habitualmente en los cuadros de ICA secundaria a una miocarditis y que progresan rápidamente al shock cardiogénico son las hipoquinesias globales, dilatación a veces de cavidades con deterioro severo de la función sistólica. En la RNM, vamos a ver los hallazgos de las miocarditis en lo que se refiere a edemas, hiperemia o fibrosis en las paredes.
¿Cuáles son las causas etiológicas que corresponden a las miocarditis? Las miocarditis pueden ser infecciosas, pueden ser bacterianas, causadas por estafilococo, estreptococo, pneumococo y meningococo entre otros. Corynebacterium y Chlamyidia también son agentes importantes en esto casos y que tiene cierta predilección por las mujeres y pacientes jóvenes también, y provoca miocarditis muy graves y con deterioro severo de la función sistólica. Las espiroquetas como la Borrelia de la enfermedad de Lyme, dentro de los hongos se puede ver Aspergillus, Actinomices, Blastomyces, Cándida, etc. Protozoos como el Tripanosoma cruzi, en nuestro caso como la enfermedad de Chagas. Otros agentes como Triquinella y las rickettsias pueden ser causantes. Con respecto a los virus, en lo que se refiere a miocarditis de tipo viral, los más comunes son los enterovirus de tipo Coxsackie A o B, ecovirus, poliovirus, influenza A y B, virus de la rubeola, de la hepatitis C y recientemente de las últimas epidemias el chikungunya y el virus Junin, Lassa etc.
Y los virus DNA como adenovirus, parvovirus, CMV, el herpes tipo 6, Epstein Barr, también pueden causarla.
Existen las miocarditis mediadas por respuesta inmune a alérgenos como son las vacunas y a drogas como penicilina, furosemida, lidocaína, isoniacida, tetraciclinas. Por aloantígenos por ejemplo el que se presenta la miocarditis del rechazo del trasplante cardiaco por autoantígenos o asociadas a enfermedad autoinmune como puede ser lupus eritematoso o sarcoidosis. También están las miocarditis tóxicas o de hipersensibilidad a drogas, a metales pesados, hormonas o agentes físicos.
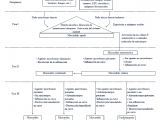
Qué sucede fisiopatogénicamente cuando ocurre una miocarditis: hay unos elementos regulatorios de la respuesta inmune como son los miocitos y las células dendríticas, hay un trigger que comienza la inflamación, que puede ser infeccioso o no infeccioso y provoca inflamación del músculo cardíaco y los síntomas que hemos descripto como dolor de pecho, insuficiencia cardíaca de distintos grados, de acuerdo al daño miocárdico producido, taquiarritimias, o cardiomiopatía aguda. Esto es la respuesta inmune que se produce por otro lado luego de la inflamación. Según esto puede haber elementos que equilibren o toleren, lo cual la hacen levemente sintomática con disminución mínima de la función sistólica del ventrículo izquierdo, o si el efecto inmune persiste hay dolores recurrentes progresión de la insuficiencia cardíaca y puede haber persistencia de la inflamación con o sin replicación viral (Fig 1).
En los protagonistas de la inflamación en el miocardio tenemos la fase de la respuesta temprana y la respuesta tardía, con la progresión de los fenómenos de inflamación y apoptposis y el camino final que es el deterioro de la función sistólica del ventrículo izquierdo. En la fase temprana hay un periodo de respuesta inmune en la cual puede haber un clearance viral con eliminación del agente causal y restauración de la función sistólica de los pacientes. De acuerdo a ese equilibrio que hay entre defensas y fenómeno inflamatorio y replicación viral, de acuerdo al daño miocárdico que produzca los grados de disfunción sistólica pueden ser aún mayores.
En otra fase más esquemática se puede ver por ejemplo que el trigger puede ser infeccioso o no infeccioso, y provocan un daño del miocito, esto provoca muerte celular, liberación de citoquinas, activación del sistema inmune, y un fenómeno de miocarditis aguda. Como dijimos en la fase 2 puede haber un clearence viral, eliminación de los agentes infecciosos y resolución de la miocarditis y esta puede estar curada. Pero también puede ser que persistan los agentes microbianos y continúe la inflamación y vaya hacia la miocarditis crónica. Y por otro lado tenemos las causas no infecciosas que también van a provocar una respuesta y ser generadores de inflamación y provocar deterioro de la función sistólica(Fig. 2).
Entonces podemos tener una miocarditis crónica microbial en la cual los agentes microbianos están presentes, no hay autoanticuerpos pero hay inflamación y destrucción celular, y esto lleva al remodelado. Tenemos una miocarditis mixta crónica que puede estar mediada por agentes microbianos e inmunes, en donde vamos a tener agentes microbianos presentes, autoanticuerpos presentes e inflamación y destrucción celular, y eso lleva también al remodelamiento.
También tenemos una miocarditis crónica autorreactiva en donde no hay agentes infecciosos pero hay anticuerpos presentes, hay inflamación y destrucción. Y posteriormente tenemos el periodo final, la miocardiopatía dilatada, en donde los agentes microbianos pueden estar presentes o no y los autoanticuerpos también pueden estar o no, pero continúa la destrucción celular y el remodelado del ventrículo izquierdo (Fig. 2).
Esto es un resumen de lo que pasa, la infección viral o bacteriana provoca infiltración linfocitaria necrosis celular, respuesta inmune para eliminar el agente causal. Puede haber autoanticuerpos, replicación viral, se perpetúan las lesiones inflamatorias y necróticas, hay disfunción sistólica y progresa a miocardiopatía dilatada.
En los fenómenos de inflamación que ocurren en la miocarditis, en lo que se refiere a los micro RNA involucrados tenemos el micro RNA del 21 al 590 que son los precursores de inflamación, y los micro RNA 221 y 222 que son más bien protectores de la inflamación. De acuerdo al balance que hay entre inflamación y replicación viral, es la magnitud del daño que puede provocar en el miocito.
Como dijimos podemos utilizar criterios histológicos e inmunohistoquímicos para el diagnóstico de miocarditis y también las imágenes del RNM ayudan mucho en el diagnóstico, los hallazgos típicos que se pueden ver son el edema de la pared y a veces parches subepicárdicos. Esto es típico de la miocarditis siempre y cuando hayamos descartado enfermedad coronaria.
Qué pasa con los métodos diagnósticos en este caso. Estamos ante una cardiomiopatía aguda inexplicable, que como en este caso requirió drogas, inotrópicas, soporte mecánico, no tuvo trastornos de conducción pero tuvo arritmias muy severas, taquicardia ventricular, y tiene insuficiencia o shock cardiogénico que no responde al manejo médico en el momento agudo. Entonces cuál es la indicación en este caso, la biopsia endomiocárdica. La biopsia endomiocárdica tiene una clase de indicación 1B. Ahora, si con el tratamiento inotrópico, drogas vasopresoras, asistencia circulatoria, el paciente se compensa y mejora, entonces valoramos en vez de la biopsia la RNM, que tiene una clase de indicación 2C.
Con respecto al tratamiento, no consideramos las miocarditis bacterianas que recibirán sus antibióticos específicos, pero sí describimos los antivirales en caso de miocarditis viral: aciclovir, ganciclovir, valganciclovir o interferón dependiendo del tipo del agente viral involucrado. Y el tratamiento inmunosupresor en los casos en los que se usan corticoides azatioprina y ciclosporina. En una serie de trials en los cuales se ensayaran los inmunosupresores. En el caso del prednisona trial fue favorable. En realidad cuando las cardomiopatías eran inflamatorias fue favorable el tratamiento inmunosupresor que habitualmente es esteroides y azatioprina o ciclosporina.
En conclusión, tenemos una paciente que se presentó con ICA, evolucionó a shock cardiogénico, tuvo disfunción multiorgánica, y muerte. Lo que pensamos como diagnóstico etiológico es una inflamación del miocardio, una miocarditis viral o bacteriana y va a haber también daños orgánicos secundarios al shock.
ANATOMÍA PATOLÓGICA
Presentamos la autopsia de una mujer de 40 años con shock cardiogénico. En la inspección externa no presentaba alteraciones a nivel de la piel, se observaba la presencia de los accesos vasculares a nivel yugular izquierdo, subclavia derecho, a nivel inguinal bilateral y una vía periférica derecha. Además presentaba una leve distensión abdominal.
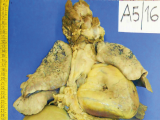
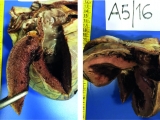
Se realizó la evisceración y fijación de todos los órganos. En la fotografía del block cardiopulmonar podemos observar la presencia de cardiomegalia (Fig 3A). La cara anterior del corazón estaba rodeado por tejido adiposo, característico del pericardio, nada que llamara la atención. A la apertura del corazón se observaba que presentaba una marcada hipertrofia, el ventrículo izquierdo medía 2 cm de espesor para un valor normal de hasta 1,5 cm. También presentaba hipertrofia del ventrículo derecho, la pared llegaba a medir hasta 1 centímetro con un valor normal hasta 0,5cm. El peso también estaba aumentado, pesaba 510 gr para un valor de alrededor de 320 gr. Se puede observar bien el engrosamiento de la pared ventricular izquierda y del tabique interventricular (Fig 3BC). Tanto las válvulas auriculoventriculares como la pulmonar y aórtica se encontraban dentro de parámetros normales.
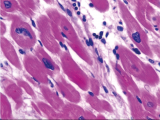
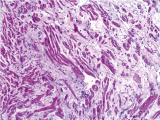
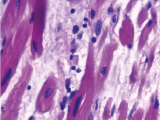
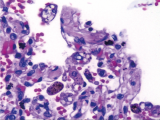
En la microscopía observamos los miocardiocitos normales con un núcleo central, y también la presencia de algunos núcleos más grandes, de bordes irregulares, y el ensanchamiento o aumento del diámetro transversal de las fibras miocárdicas. Esto es lo característico de la hipertrofia cardíaca (Fig 4). En el corte transversal se observan las mismas características, los núcleos bien globulosos. Además observamos en algunas áreas la presencia de un edema intersticial, lo cual producía la separación de las células musculares, y en algunas áreas se observa que este edema era bastante abundante (Fig 5).
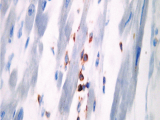
En algunas áreas también se observa la presencia de un infiltrado inflamatorio y se ven células mononucleares correspondientes a linfocitos y algunas células plasmáticas. En algunas áreas este infiltrado era un poco más denso, e intenta introducirse dentro de las fibras musculares (Fig. 6A). A mayor aumento se puede observar que las células infamatorias eran de tipo mononuclear. Ante esto solicitamos técnica de inmunohistoquímica. Como dijo el doctor Estrada uno se debe ayudar con la inmunohistoquímica para diferenciar si estos infiltrados inflamatorios son fisiológicos o patológicos. Pedimos CD45 que marca las membranas de los linfocitos y se observa que son más de 14 células (Fig. 6B).
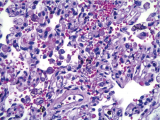
Ante esto teníamos un diagnóstico de una miocarditis. Dentro de la clasificación de Dallas era una miocarditis de tipo borderline, ya que no presentaba ni degeneración de las fibras musculares ni tampoco se observaba necrosis. Nos ayudamos con la técnica de inmunohistoquímica confirmando que tampoco era un infiltrado de tipo fisiológico. En el corte del pericardio observamos que presentaba un engrosamiento por la fibrosis. La citología del líquido pericárdico contenía células inflamatorias mononucleares con linfocitos y células plasmáticas correspondientes a una citología inflamatoria. En la macroscopía del sistema respiratorio se apreciaba una superficie externa de coloración grisáceo con puntillado negruzco que sería vinculable macroscópicamente a antracosis. Tanto el peso como las medidas se encontraban dentro de parámetros normales. En los hilios del pulmón descartamos un embolismo ya que no se observaba ningún coágulo adherido a los vasos. En el corte de la microscopía del pulmón, se apreciaba un engrosamiento de los tabiques alveolares, esto se debe al infiltrado inflamatorio mononuclear y a mayor aumento se observa la presencia de extravasación eritrocitaria y también de hemosiderofagos (Fig. 7 AB)
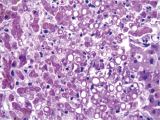
El hígado pesaba 1.100 kg para valores normales de 1.400, es decir no presentaba hepatomegalia y medidas eran normales, con una superficie lisa. En la microscopía lo característico era una necrosis de tipo centrolobulillar típica del shock. Todas las áreas alrededor de la vena central son áreas de necrosis y las más violáceas son hepatocitos que todavía están viables porque reciben el flujo de sangre de los espacios porta. A mayor aumento se puede apreciar la necrosis y los hepatocitos que continúan viables y los cambios reparativos que presenta el hígado que es la esteatosis (Fig. 8).
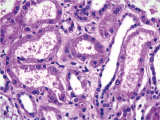
Respecto al sistema urinario, realizamos la apertura del riñón y se observa la palidez de la corteza con un poco de congestión a nivel de la médula, que también es lo típico de un riñón de shock. Los dos uréteres que no presentaban alteraciones y la vejiga. Lo típico, lo que nosotros esperamos encontrar en la microscopía de estos riñones es necrosis tubular aguda, y fue lo que encontramos. Estos son todos los túbulos que se encuentran revestidos por células cúbicas y se observa la pérdida de los núcleos, es decir la necrosis de estas células con el desflecamiento (Fig. 9). Incluso algunas veces se pueden encontrar los cilindros en el interior, que es lo característico de la necrosis tubular aguda en estos pacientes.
La médula ósea era normal, el compartimento medular presentaba las células adiposas y las series hematopoyéticas encontraban conservadas y sin hemofagocitosis.
Los hallazgos de la autopsia fueron: cardiomegalia de 510 gr, con hipertrofia ventricular izquierda de 2 cm, una miocarditis borderline según la clasificación de Dallas; neumonía intersticial crónica, edema y hemorragia focal intraalveolar; hígado con necrosis centrolobulillar y riñón con necrosis tubular aguda. La causa probable de muerte es shock cardiogénico secundario a miocarditis y riñón e hígado de shock. Uno de los hallazgos, a modo anecdótico, fue una leiomioma a nivel del útero.
Ahora vamos a ver los métodos complementarios. En la autopsia como estábamos en comunicación con los cardiólogos y sabíamos que existía una sospecha de miocarditis se envió a histocompatibilidad una muestra de miocardio.
BIOLOGÍA MOLECULAR
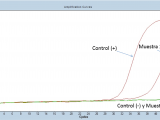
Recibimos una pieza de miocardio de la cual aislamos los ácidos nucleicos y le hicimos técnicas de biología molecular, específicamente PCR convencional y en tiempo real para los diferentes patógenos: enterovirus, adenovirus, Chagas, herpes 6, Epstein Barr, H1N1, micoplasma pneumoniae y clamidia pneumoniae. El resultado fue positivo para parvovirus B19. En la imagen se ve el control interno en el aparato de real time donde en ese momento habíamos analizado dos pacientes. El paciente 1 es el paciente en cuestión que se discutió hoy, y el paciente 2 era otra muestra y lo que podemos ver es la amplificación de un control interno para validar la reacción. Tenemos los controles internos de ambos pacientes, un control interno de reacción y el control negativo que nos dice que está bien la reacción, que no hay contaminación (Fig 10A).
En la amplificación en el canal específico que nos va a dar el parvovirus donde tenemos el control positivo que tiene señal, una señal fuerte, bien clara, al igual que el paciente 1 que era el paciente que estamos discutiendo hoy y el paciente 2 y el control negativo en verde están sin fluorescencia, eso quiere decir que no tiene y es no detectable (Fig 10B).
DIAGNOSTICO FINAL:
Shock cardiogénico secundario a miocarditis por Parvovirus B19.