Volumen 33, Nº 1 | 2015
Neuroblastoma neonatal estadío IV: abordaje quirúrgico de emergencia - Stage IV neonatal neuroblastoma: emergency surgical approach
Víctor Defagó, Adriana Berreta, Ariel Sferco, Carlos Hollman
Palabras clave: neuroblastoma estadío IV, Recién nacido, Silo, Resección hepática.
Keywords: stage IV neuroblastoma, newborn, silo, hepatic resection.
INTRODUCCIÓN
Los pacientes con neuroblastoma neonatal estadío IV (NBT IV) pueden presentar implantes hepáticos que crecen rápidamente y generan una gran presión intraabdominal llegando a comprometer la vida del paciente.
Una situación similar se observa en los pacientes con estadío IV-S, aunque su pronóstico es mejor (1,2). La infiltración difusa del hígado puede ser controlada con quimioterapia o radioterapia. La utilización de un silo abdominal tiene el propósito de disminuir la presión del abdomen en el paciente crítico, facilitando así el tiempo de espera hasta que retrograden el tumor y las metástasis hepáticas. Si bien la técnica del silo fue descripta anteriormente, no fue aplicada con frecuencia por complicaciones inherentes a la malla, tales como infección y/o dehiscencia de la sutura que pueden amenazar la vida del paciente (3,4). La reducción quirúrgica del parénquima hepático surgió como alternativa para un paciente crítico en el cual se necesitaba disminuir rápidamente el contenido abdominal, y además acortar el período de tiempo del silo para facilitar el cierre precoz de la pared abdominal.
El objetivo de este trabajo es presentar el tratamiento de un neonato con neuroblastoma estadío IV que necesitó un silo abdominal, y reducción hepática quirúrgica para lograr el cierre precoz y definitivo del abdomen.
DESCRIPCIÓN DEL CASO
Paciente que ingresa a los 14 días de vida con hepatomegalia e insuficiencia respiratoria. La tomografía computada mostró tumor en glándula suprarrenal izquierda e infiltración difusa del hígado. Los niveles de ferritina, enolasa y ácido vanil mandélico estaban elevados. La punción medular mostró una infiltración del 25%. La biopsia hepática confirmó el diagnóstico de neuroblastoma estadío IV. A los 20 días de vida presentó insuficiencia respiratoria y fallo hepático. Se inició el tratamiento quimioterápico con ciclofosfamida sin lograr respuesta objetiva.
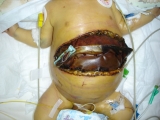
Debido a la imposibilidad de ventilación por la excesiva presión abdominal, se realizó resección no anatómica del 35% del parénquima hepático y se confeccionó un silo de polietileno (Figura 1).
La histopatología confirmó el diagnóstico de neuroblastoma pobremente diferenciado, con escaso estroma, índice mitótico >10 (Shimada) y amplificación del N-Myc. Requirió la administración de factor VII activado para corregir las alteraciones en la coagulación debido a la insuficiencia hepática en el período
postoperatorio.
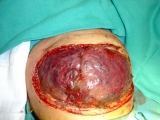
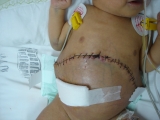
Se realizó diálisis peritoneal a través del drenaje abdominal que se había colocado a causa de su hemoperitoneo. Fue incluído en protocolo SIOP para neuroblastoma en niños menores de un año y de alto riesgo (Régimen CADO). La mejoría clínica del paciente permitió la extracción del silo (Figura 2) y
el cierre definitivo de la pared abdominal a los 44 días de vida (Figura 3).
A los 3 meses se indicó la resección del tumor primario localizado en glándula suprarrenal izquierda. Finalizó su tratamiento de acuerdo al protocolo que incluyó quimioterapia en altas dosis con rescate de células madres autólogas. A los 5 años de edad se encuentra libre de enfermedad, con un hígado de tamaño y función normal.
DISCUSIÓN
En el neuroblastoma, la edad es un factor pronóstico y se considera que ser menor de un año es favorable. Sin embargo, en la etapa neonatal las metástasis hepáticas suelen infiltrar el órgano en forma difusa generando un crecimiento inusual del hígado que conduce a una situación crítica que amenaza la vida del paciente, al provocar un fallo multiorgánico por la excesiva presión intraabdominal. En esta situación se deben tomar medidas
de salvataje que no están exentas de riesgos colaterales.
La descompresión abdominal es una opción para mejorar la ventilación en esta situación grave (2). Si bien esta técnica fue originalmente aplicada a los pacientes con neuroblastoma IV-S, pareció conveniente aplicar la misma estrategia para el estadío IV mediante la generación de una hernia abdominal
controlada con un silo de material sintético que permitió alojar temporariamente al hígado mientras se disminuía la presión intraabdominal.
Esta estrategia no está libre de complicaciones causadas por infecciones o dehiscencias del silo (2). Se han publicado últimamente artículos que destacan las bondades de la descompresión abdominal utilizando diferentes materiales (5,6) y técnicas que incluyen la presión negativa (7). Parece ser que lo más importante es la descompresión y no tanto los materiales utilizados, ya que el éxito dependería de la evolución misma de la enfermedad (8).
En este paciente se privilegió la descompresión confeccionando un silo con bolsas de polietileno que se mantuvo durante los momentos más críticos. Al lograr la estabilidad hemodinámica se comenzó el proceso de reducción de tamaño del silo mediante el plegado progresivo hasta lograr el afrontamiento de ambos bordes de la pared abdominal.
Con respecto a la reducción hepática para disminuir el volumen de contenido abdominal y acelerar los tiempos del cierre de la pared, no hemos encontrado respaldo bibliográfico que sostenga la postura adoptada. Las experiencias más parecidas se refieren a metástasis hepáticas localizadas en niños mayores de 4 meses, en los cuales se practicaron resecciones hepáticas anatómicas (9,10). En este niño, el hígado era una gran masa rígida que estaba infiltrada por tejido tumoral y comprimía todos los órganos abdominales con elevación severa del diafragma.
La idea de resecar parénquima hepático para disminuir su volumen es atractiva ya que no solo mejoraría la situación de estos pacientes críticos en cuanto a la dificultad del manejo ventilatorio y del fallo multiorgánico sino que se acelerarían los tiempos para el cierre de la pared abdominal, disminuyendo el riesgo de complicaciones por el uso prolongado de estas prótesis cuya aplicación tiene un tiempo limitado.
En este paciente, al realizar la hepatectomía parcial, fuemuy difícil respetar exactamente los segmentos por lo que se priorizó la resección no anatómica extrayendo más de un tercio del hígado. En estudios posteriores se observó la desaparición de los implantes y la regeneración del parénquima hepático.
La cirugía del tumor primitivo residual se basó en los criterios del INSS (11) que sugieren que en los pacientes con neuroblastoma estadío IV está indicada la resección del tumor primario persistente al finalizar la quimioterapia.
CONCLUSIONES
En pacientes críticos, la confección transitoria de un silo de material sintético permite mantener la vida del neonato al descomprimir el abdomen, mejorar la ventilación y disponer de más tiempo para el tratamiento quimioterápico mientras se espera la evolución tumoral.
La reducción del parénquima hepático comprometido puede ser una alternativa para mejorar la situación crítica del paciente y acelerar el cierre de la pared abdominal disminuyendo el riesgo de complicaciones.
Bibliografía
1. Elimam NA, Atra AA, Fayea NY, et al. Stage 4S neuroblastoma, a disseminated tumor with excellent outcome. Saudi Med J 27: 1734-1736, 2006.2. Nickerson HJ,Nesbit ME,Grosfeld JL, et al. Comparison of stage IV and IV-S neuroblastoma in the first year of life. Med Pediatr Oncol 13:261-268, 1985
3. Müller-Berghaus J, Kurowski C, Gharib M , et al. Artificial abdominal hernia for the treatment of hepatomegaly in a neonate with stage 4s neuroblastoma. Pediatr Hematol Oncol 16:453-458, 1999.
4. Nickerson JH, Matthay KK, Seeger RC, et al. Favorable biology and outcome of stage IV-S neuroblastoma with supportive care or minimal therapy: a Children´s Cancer Group Study. J Clin Oncol 18: 477-486, 2000. Trabajos originales 09
5. Keene DJ, Minford J, Craiqie RJ, et al. Laparostomy closure in stage 4s neuroblastoma. J Ped Surg 46: e 1- 4, 2011.
6. Mc Gahren ED, Rodgers BM, Waldron PE, et al. Successful management of stage 4S neuroblastoma and severe hepatomegaly
using absorbable mesh in an infant. J Pediatr Surg 33: 554-1557, 1998.
7. Roberts S, Creamer K, Shoupe B, et al. Unique management of stage 4S neuroblastoma complicated by massive hepatomegaly: case report and review of the literature. J Pediatr Hematol Oncol 24: 142-144, 2002.
8. Harper L, Perel Y, Lavrand F, et al. Surgical management of neuroblastoma-related hepatomegaly: do material and method really count? Pediatr Hematol Oncol 25: 313-317, 2008.
9. Tannuri AC, Tannuri U, Gibelli NE, et al. Surgical treatment of hepatic tumors in children, lessons learned from liver transplantation. J Pediatr Surg 44 :2083-2087, 2009.
10. Su WT, Rutigliano DN, Gholizadeh M, et al. Hepatic metastasectomy in children. Cancer 109 : 2089-2092, 2007.
11. Joshi V V. Peripheral Neuroblastic Tumors: Pathologic Classification Based on Recommendations of International Neuroblastoma Pathology Committee (modification of Shimada Classification). Department of Pediatric Pathology, Connecticut Children’s Medical Center and Hartford Hospital. Pediatric and Developmental Pathology 3: 184-199, 2000.